当前位置: /首页 /人才队伍 /学术队伍 /常凌乾 /最新成果 /正文
临床上,当皮肤创面超过6平方厘米时,其修复速度将显著慢于小创口,且易引起并发症,如伤口感染等。传统治疗皮肤创伤的方法,主要基于敷料、表皮移植和细胞外基质支架。这些方法在伤口愈合过程中,主要经历三个关键过程:1)结痂形成,建立止血和防外环境的屏障;2)结痂下的表皮细胞增殖和迁移,导致创面闭合;3)表皮下的成纤维细胞和内皮细胞增殖、迁移和功能化,实现真皮重塑。
然而,对于大面积创伤,这些方法很难控制这三个过程的转变,尤其是表皮与真皮再生方面,面临着巨大挑战,最终导致再生皮肤在创面处结构紊乱和功能丧失。
针对这一问题,北京航空航天大学常凌乾联合团队设计了一种表贴式生物电子器件,称为E-TASHI,可以精确控制三个阶段的过渡,为大面积皮肤伤口提供加速和空间均衡愈合。相关成果以“A Degradable Bioelectronic Scaffold for Localized Cell Transfection toward Enhancing Wound Healing in a 3D Space”为题,发表在《Advanced Materials》上。论文通讯作者还包括北京航空航天大学牟玮教授、香港城市大学于欣格教授、中国中医科学院王毅研究员、国家卫生健康委科学技术研究所尹德东研究员。论文第一作者包括博士研究生肖傲、蒋欣然,北大第一医院胡永艳博士,香港城市大学李虎博士和焦艳丽。

研究团队设计的可降解-细胞电转生物电子支架(E-TASHI),质量约为8克,由两个功能模块组成: 1)质粒电转染模块,该模块携带供电系统,可在短时间(<1分钟)启动脉冲电场,实现伤口边缘细胞电穿孔,并递送质粒(编码促细胞增殖和迁移的基因质粒)进入细胞,促进细胞的快速增值和迁移到支架模块的孔隙内。2)细胞支架模块,由可生物降解的水凝胶组成的多孔状结构,在短时间内可降解为氨基酸为生物体利用。支架的孔状结构类似细胞外基质,为细胞生长和迁移提供微环境和力学支撑。在伤口修复过程中,有利于真皮层细胞在伤口垂直深度内的分布和生长分化,从而实现表皮(平面)和真皮(空间)修复的同步推进,最终创面重建完整皮肤结构,形成的愈合皮肤与健康皮肤高度相似(图1)。
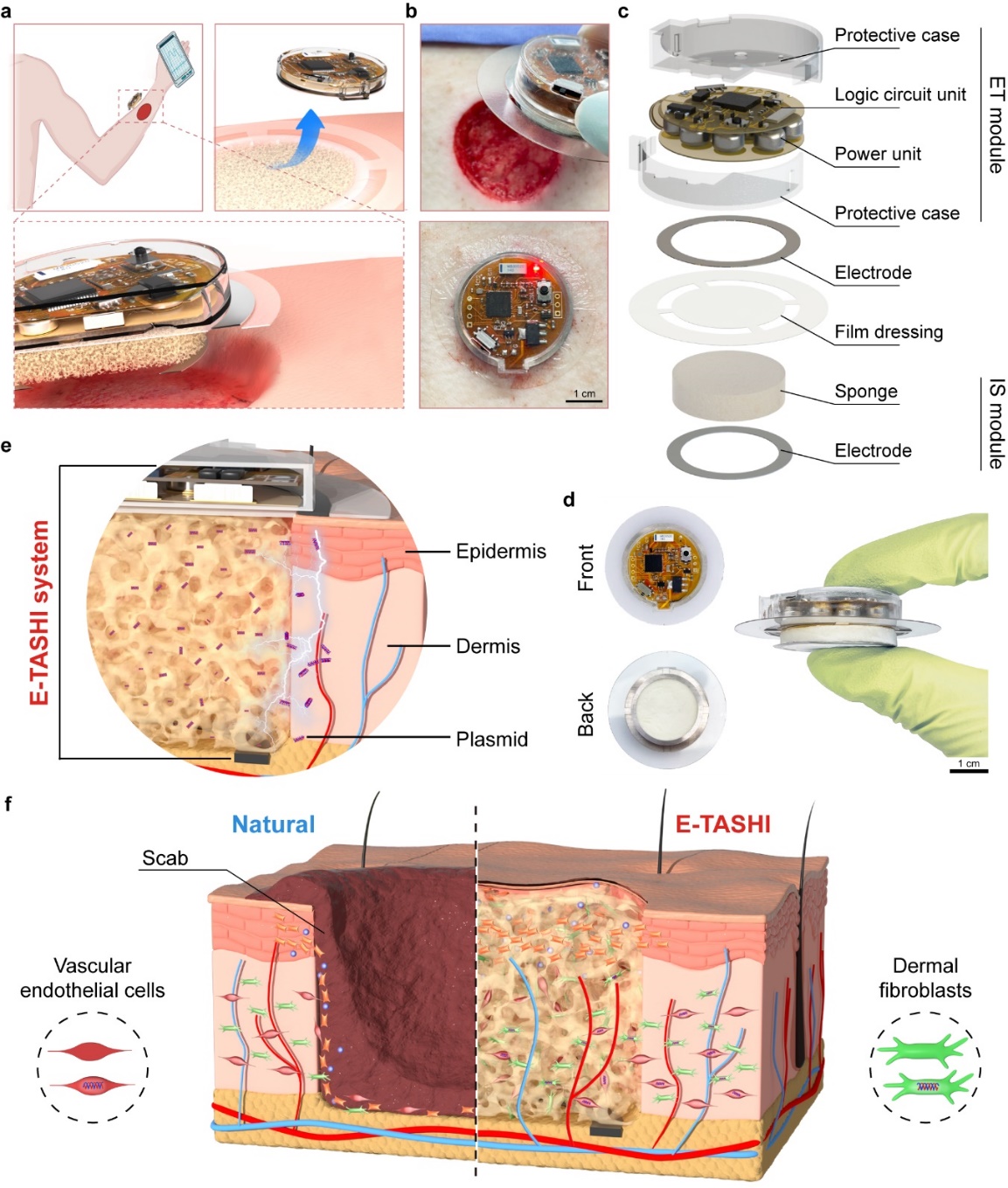
图1.E-TASHI器件利用支架和电转染双重功效,实现大创口的空间均衡愈合和修复。
为了评估E-TASHI在创面的伤口修复能力,研究者们建立了大鼠创伤模型。将E-TASHI植入创面,执行电转染操作。通过检测与创面愈合相关指标在7,14和28天的变化,发现细胞数量、血管数量等指标在7天时达到峰值,创面修复进入高峰期;在14天细胞与血管数量减少,创面修复接近尾声,且与健康状态下的细胞与血管数量无显著差距。胶原沉积分数和胶原排列方向也在14天时与健康状态下无显著差异。在28天时创面皮肤切面与健康皮肤高度相似(图2)。
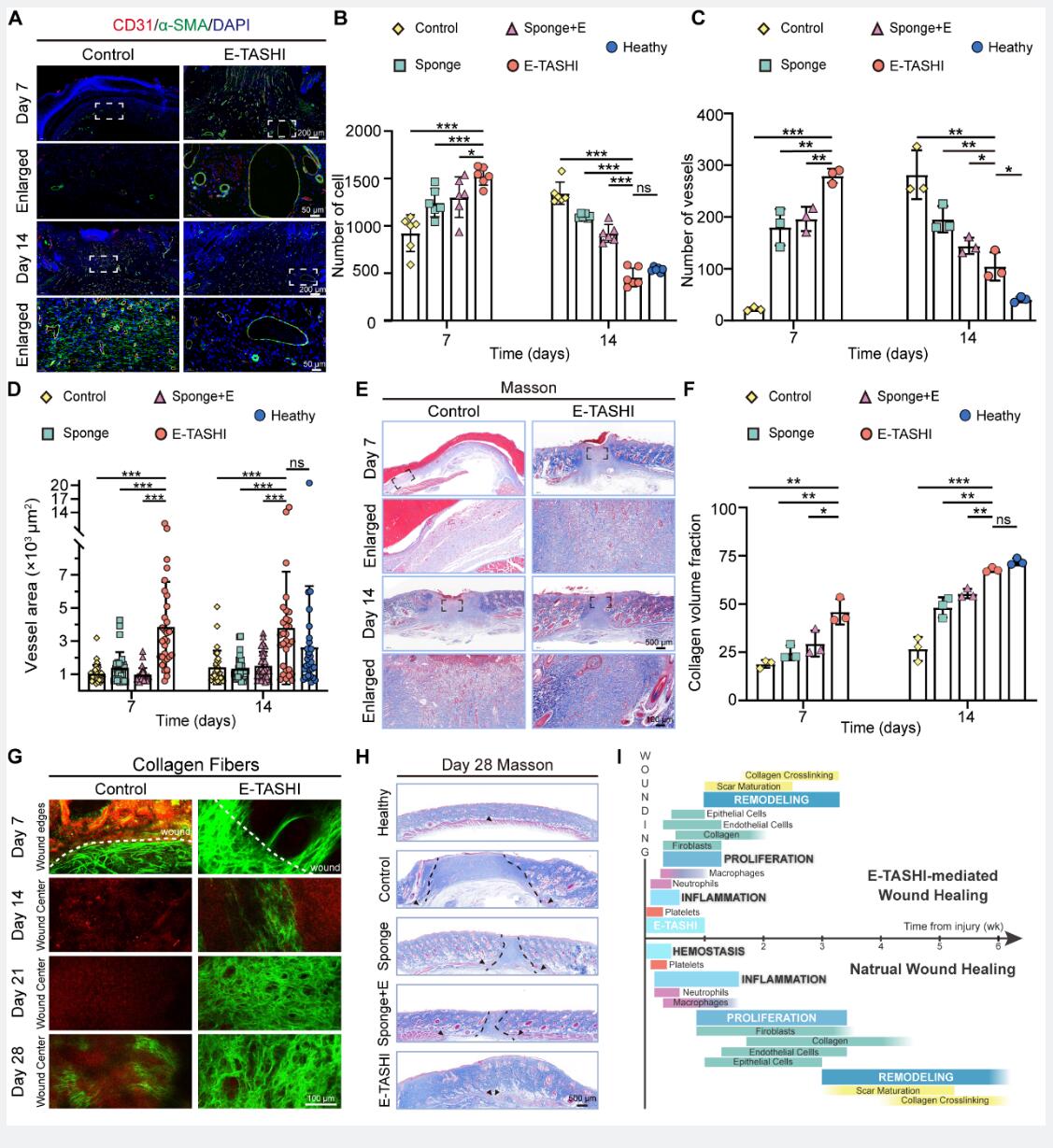
图2. E-TASHI治疗大鼠创面,创口处与愈合相关的指标变化。
最后,研究团队在巴马猪模型上进一步验证了E-TASHI在创面的伤口修复能力。与大鼠创面修复结果类似,E-TASHI在28天时创面愈合面积几乎完成,细胞数量、血管数量和胶原沉积分数等指标也与健康组无显著性差异(图3)。
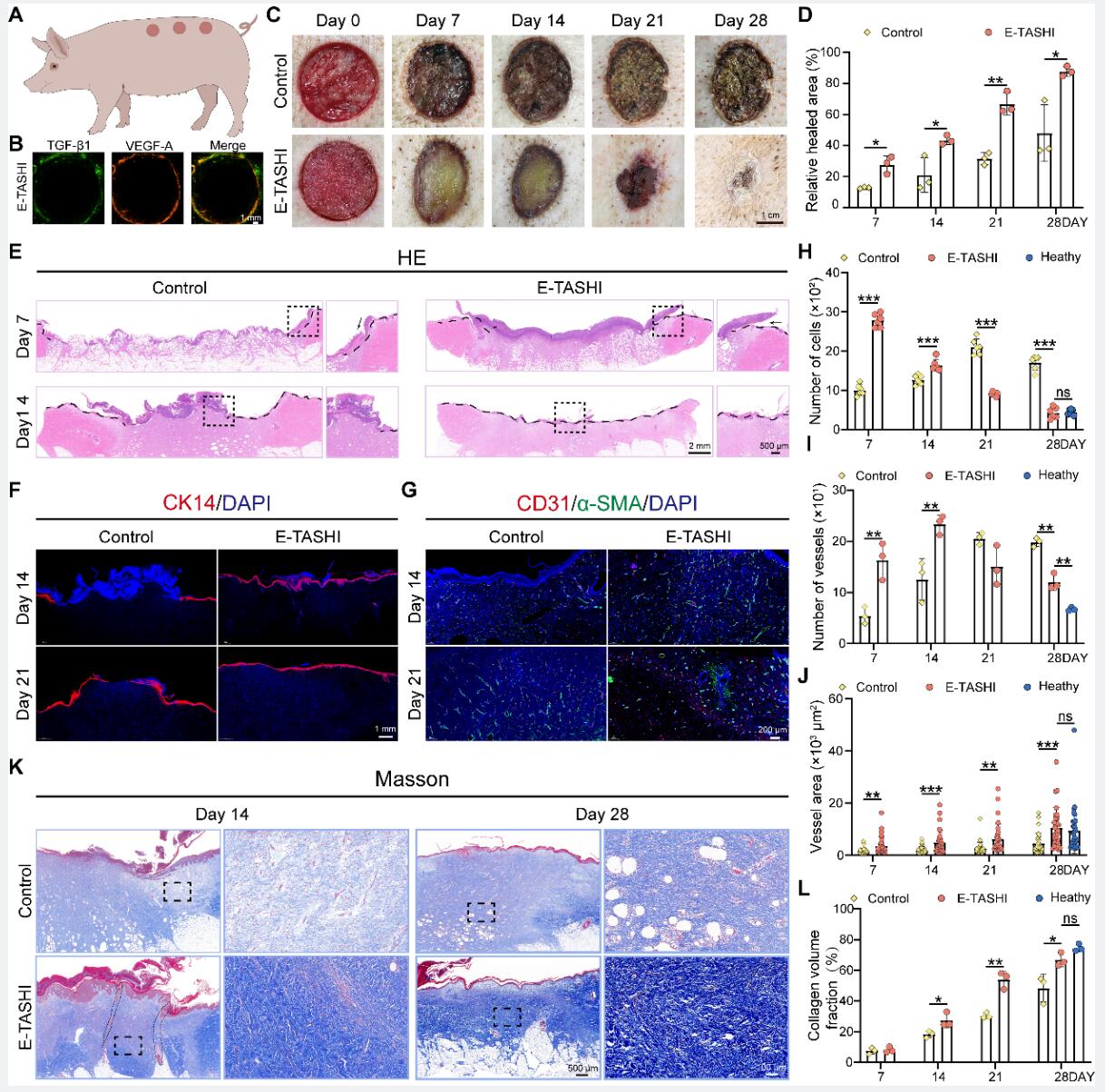
图3. 巴马猪创面修复模型,创面修复相关指标变化。
该电子器件中细胞支架部分在完成细胞增殖和皮肤愈合后,完全降解,无需二次取出;同时,研究团队‘从大创口中不同层细胞增殖速度不同,导致愈合不均衡’这一科学问题出发,设计了原位自供电转染微纳器件,为大创面空间均衡修复提供了一种另辟蹊径的高效修复途径。
文章链接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202404534